comment sont fabriqués les vaccins antigrippaux
- vaccins antigrippaux à base D’œufs
- vaccins antigrippaux à base de cellules
- vaccins antigrippaux recombinants
pour les États-Unis, il existe trois technologies différentes de production de vaccins antigrippaux approuvées par la Food and Drug Administration (FDA) des États-Unis icône externe:
- vaccin antigrippal à base d’œufs,
- vaccin antigrippal à base de cellules et
- vaccin antigrippal recombinant.,
tous les vaccins antigrippaux disponibles dans le commerce aux États-Unis sont fabriqués par des fabricants du secteur privé. Différents fabricants utilisent différentes technologies de production, mais tous les vaccins contre la grippe répondent aux exigences de sécurité et d’efficacité de la FDA. Différents vaccins ont des indications différentes. Voir vaccins antigrippaux-États-Unis, saison grippale 2019-2020 pour des indications spécifiques.
vaccins antigrippaux à base d’œufs
la façon la plus courante de fabriquer des vaccins antigrippaux est d’utiliser un procédé de fabrication à base d’œufs
utilisé depuis plus de 70 ans., La fabrication de vaccins à base d’œufs est utilisée pour fabriquer à la fois un vaccin inactivé (tué) (généralement appelé « vaccin antigrippal”) et un vaccin vivant atténué (affaibli) (généralement appelé « vaccin antigrippal par pulvérisation nasale”).
le processus de production à base d’œufs commence par le CDC ou un autre partenaire de laboratoire du système mondial de Surveillance et de réponse grippales de l’OMS fournissant aux fabricants du secteur privé des virus candidats-vaccins (CVV) cultivés dans des œufs conformément aux exigences réglementaires actuelles de la FDA., Ces CVV sont ensuite injectés dans les œufs de poule fécondés et incubés pendant plusieurs jours pour permettre aux virus de se répliquer. Le liquide contenant le virus est récolté à partir des œufs. Pour les vaccins antigrippaux inactivés (c.-à-d. les vaccins antigrippaux), les virus vaccinaux sont ensuite inactivés (tués) et l’antigène viral est purifié. Le processus de fabrication se poursuit avec des tests de qualité, le remplissage et la distribution. Pour le vaccin antigrippal par pulvérisation nasale (c. – à-d. le vaccin antigrippal vivant atténué-VVAI), les VVV de départ sont des virus vivants, mais affaiblis qui passent par un processus de production différent., La FDA teste et approuve tous les vaccins antigrippaux avant la libération et l’expédition.
Il existe plusieurs fabricants différents qui utilisent cette technologie de production pour fabriquer des vaccins contre la grippe aux États-Unis. Cette méthode de production nécessite un grand nombre d’œufs de poule pour produire le vaccin et peut prendre plus de temps que d’autres méthodes de production.
vaccins contre la grippe à base de cellules
Il existe également un processus de production à base de cellules pour les vaccins contre la grippe qui a été approuvé par la FDA en 2012. Jusqu’à récemment, ce processus de production a également commencé avec des CVV cultivés sur des œufs conformément aux réglementations de la FDA., Cependant, le 31 août 2016, la FDA a approuvé Seqirus, le seul fabricant de vaccins antigrippaux à base de cellules approuvé PAR LA FDA aux États-Unis, pour commencer à utiliser des CVV à base de cellules. La fabrication cellulaire est utilisée pour fabriquer des vaccins antigrippaux inactivés (p. ex., le vaccin antigrippal).
le processus de création de vaccins antigrippaux cellulaires comporte plusieurs étapes. Tout d’abord, le CDC ou l’un de ses partenaires de laboratoire utilisent des virus grippaux cultivés dans des cellules pour fabriquer des CVV, qui sont ensuite fournis à un fabricant de vaccins., Ensuite, le fabricant du vaccin inocule les CVV dans des cellules de mammifères en culture (plutôt que dans des œufs) et permet aux CVV de se reproduire (c.-à-d. de faire des copies) pendant quelques jours. Ensuite, le liquide contenant le virus est collecté à partir des cellules et l’antigène du virus est purifié. Le processus de fabrication se poursuit avec la purification et les tests. Enfin, la FDA teste et approuve les vaccins avant leur libération et leur expédition.
la production cellulaire de vaccins contre la grippe ne nécessite pas d’œufs de poule, car les virus utilisés pour fabriquer le vaccin sont cultivés dans des cellules animales., La technologie cellulaire a également le potentiel d’accélérer le démarrage du processus de fabrication du vaccin contre la grippe.
bien que les virus utilisés dans le vaccin cellulaire des saisons précédentes aient été cultivés dans des cellules, avant la saison 2019-2020, certains des virus fournis au fabricant provenaient à l’origine d’œufs. Pour la saison grippale 2019-2020, les quatre virus de la grippe utilisés dans le vaccin à base de cellules sont dérivés de cellules, ce qui rend le vaccin exempt d’œufs.
pour plus d’informations, consultez la page Web des vaccins antigrippaux cellulaires des CDC.,
vaccins recombinants contre la grippe
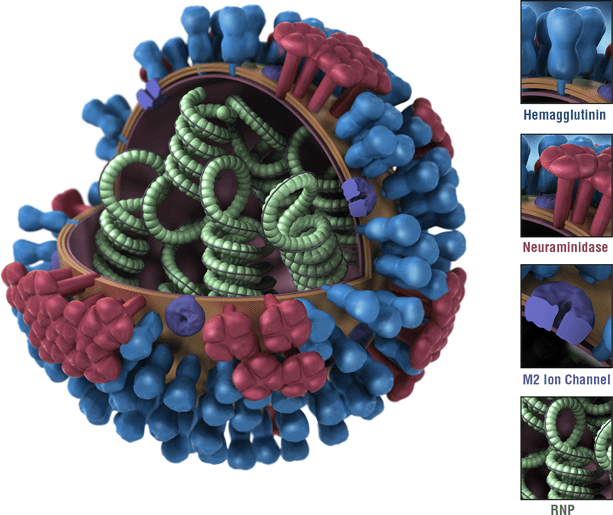
Il s’agit d’une image d’un virus grippal. Les protéines de surface de l’hémagglutinine (HA) du virus sont représentées en bleu. Les a D’un virus de la grippe sont des antigènes. Les antigènes sont des caractéristiques du virus de la grippe qui sont reconnues par le système immunitaire et qui déclenchent une réponse immunitaire protectrice. La plupart des vaccins contre la grippe sont conçus pour déclencher une réponse immunitaire contre la HAs des vaccins antigrippaux en circulation.,
Il existe une troisième technologie de production pour les vaccins contre la grippe qui a été approuvée pour utilisation sur le marché américain en 2013 et qui implique l’utilisation de la technologie recombinanteexternal icon. Les vaccins antigrippaux recombinants ne nécessitent pas la production d’un échantillon de virus candidat-vaccin (CVV). Au lieu de cela, les vaccins recombinants sont créés synthétiquement. Pour fabriquer un vaccin recombinant, les scientifiques de la grippe obtiennent d’abord de l’ADN, c’est-à-dire des instructions génétiques, pour fabriquer une protéine de surface appelée hémagglutinine (HA) présente sur les virus de la grippe., HA est un antigène, qui est une caractéristique d’un virus de la grippe qui déclenche le système immunitaire humain pour créer des anticorps qui ciblent spécifiquement le virus. Cet ADN pour fabriquer l’antigène HA du virus de la grippe est ensuite combiné à un baculovirus, un virus qui infecte les invertébrés. Il en résulte un virus « recombinant ». Le rôle du baculovirus est d’aider à transporter les instructions D’ADN pour fabriquer l’antigène HA du virus de la grippe dans une cellule hôte. Une fois que le virus recombinant pénètre dans une lignée cellulaire hôte qualifiée par la Food and Drug Administration (FDA), il demande aux cellules de produire rapidement l’antigène HA., Cet antigène est cultivé en vrac, collecté, purifié, puis emballé sous forme de vaccin recombinant contre la grippe. La qualité et la puissance de ces vaccins sont ensuite testées par la FDA avant que celle-ci n’approuve la diffusion des lots de vaccins au public.
Cette méthode de production ne nécessite pas de virus vaccinal cultivé sur des œufs et n’utilise pas du tout d’œufs de poule dans le processus de production. Bien qu’il existe d’autres vaccins sur le marché américain qui utilisent des procédés de fabrication recombinants similaires, il n’y a qu’un seul vaccin antigrippal produit à l’aide d’une technologie recombinante approuvée par la FDA pour une utilisation aux États-Unis à l’heure actuelle., Ce processus de production est le plus rapide car il n’est pas limité par la sélection de virus vaccinaux adaptés à la croissance dans les œufs ou au développement de virus vaccinaux à base de cellules.
les CDC et la FDA surveillent l’innocuité de tous les vaccins autorisés aux États-Unis, y compris les vaccins contre la grippe saisonnière. De plus amples renseignements sur l’innocuité de la grippe à base d’œufs, de cellules et de recombinaison, y compris les effets indésirables, les contre-indications et les précautions, Le dépistage et l’administration sécuritaire du vaccin sont disponibles à L’adresse suivante: sécurité des vaccins contre la grippe saisonnière: Résumé à l’intention des cliniciens.,
- L’évolution et la révolution des vaccins contre la Grippecône externe sur le site Web de la Food and Drug Administration des États-Unis.
- recherche sur le vaccin contre la Grippecône externe sur le site Web du National Institute of Allergy and Infectious Diseases Institute,NIH.
- Vaccin contre la Grippe Avancées















