Hoe worden griepvaccins gemaakt
- Eigebaseerde griepvaccins
- celgebaseerde griepvaccins
- Recombinant griepvaccins
voor de Verenigde Staten zijn er drie verschillende productietechnologieën voor griepvaccins goedgekeurd door de Amerikaanse Food and Drug Administration (FDA) ul>
alle in de handel verkrijgbare griepvaccins in de Verenigde Staten worden gemaakt door producenten uit de particuliere sector. Verschillende fabrikanten gebruiken verschillende productietechnologieën, maar alle griepvaccins voldoen aan de veiligheids-en effectiviteit-eisen van de FDA. Verschillende vaccins hebben verschillende indicaties. Zie influenzavaccins-Verenigde Staten, 2019-2020 Influenzaseizoen voor specifieke indicaties.
griepvaccins op basis van eieren
de meest voorkomende manier waarop griepvaccins worden gemaakt is met behulp van een productieproces op basis van eieren
dat al meer dan 70 jaar wordt gebruikt., De productie van vaccins op basis van eieren wordt gebruikt om zowel geïnactiveerd (gedood) vaccin (meestal de “griepprik” genoemd) als levend verzwakt (verzwakt) vaccin (meestal het “neusspray griepvaccin”genoemd) te maken.
het productieproces op basis van eieren begint met CDC of een andere laboratoriumpartner in het who Global Influenza Surveillance and Response System die particuliere fabrikanten voorziet van kandidaatvaccinvirussen (CVV ‘ s) die in eieren worden gekweekt volgens de huidige FDA-regelgeving., Deze CVV ‘ s worden vervolgens geïnjecteerd in bevruchte kippeneieren en geïncubeerd voor meerdere dagen om de virussen te repliceren. De vloeistof die het virus bevat, wordt uit de eieren geoogst. Voor geïnactiveerde influenzavaccins (d.w.z. griepvaccins) worden de vaccinvirussen vervolgens geïnactiveerd (gedood) en wordt het virusantigeen gezuiverd. Het productieproces gaat verder met kwaliteitstesten, vullen en distribueren. Voor het neusspray griepvaccin (d.w.z. het levend verzwakt griepvaccin – LAIV) zijn de beginnende CVV ‘ s levende, maar verzwakte virussen die een ander productieproces doorlopen., FDA test en keurt alle influenzavaccins goed voorafgaand aan release en verzending.
Er zijn verschillende fabrikanten die deze productietechnologie gebruiken om griepvaccins te maken voor gebruik in de Verenigde Staten. Deze productiemethode vereist grote aantallen kippeneieren om vaccin te produceren en kan langer duren dan andere productiemethoden.
op cellen gebaseerde griepvaccins
Er is ook een op cellen gebaseerd productieproces voor griepvaccins dat in 2012 door de FDA is goedgekeurd. Tot voor kort begon dit productieproces ook met eigekweekte CVV ‘ s per FDA-regelgeving., Echter, op 31 augustus 2016, gaf de FDA een goedkeuring voor Seqirus, de enige FDA-goedgekeurde cel-gebaseerde griepvaccin fabrikant in de Verenigde Staten, om te beginnen met behulp van cel-gekweekte CVV ‘ s. Cell-based manufacturing wordt gebruikt om geïnactiveerde griepvaccins te maken (bijvoorbeeld het griepprik).
het proces van het aanmaken van op cellen gebaseerde griepvaccins omvat verschillende stappen. Eerst gebruiken CDC of een van haar laboratoriumpartners influenzavirussen die in cellen zijn gekweekt om CVV ‘ s te maken, die vervolgens aan een vaccinfabrikant worden verstrekt., Vervolgens vaccineert de vaccinfabrikant de CVV ’s in gekweekte zoogdiercellen (in plaats van in eieren) en laat hij de CVV’ s een paar dagen repliceren (d.w.z. kopieën maken). Vervolgens wordt de virusbevattende vloeistof uit de cellen verzameld en wordt het virusantigeen gezuiverd. Het productieproces gaat verder met zuivering en testen. Tot slot test en keurt de FDA de vaccins goed voordat ze worden vrijgegeven en verzonden.
de productie van griepvaccin op Celbasis vereist geen kippeneieren omdat de vaccinvirussen die worden gebruikt om het vaccin te maken, in dierlijke cellen worden gekweekt., Celgebaseerde technologie heeft ook het potentieel voor een snellere start van het productieproces van griepvaccins.
terwijl virussen die in voorgaande seizoenen op cellen gebaseerd vaccin werden gebruikt, in cellen werden gekweekt, waren vóór het seizoen 2019-2020 enkele van de aan de fabrikant verstrekte virussen oorspronkelijk afkomstig uit eieren. Voor het influenzaseizoen 2019-2020 zijn alle vier de griepvirussen die in het celgebaseerde vaccin worden gebruikt, cel-afgeleid, waardoor het vaccin eivrij is.
voor meer informatie, zie CDC ‘ s cell-Based Flu Vaccines webpage.,
Recombinant griepvaccins
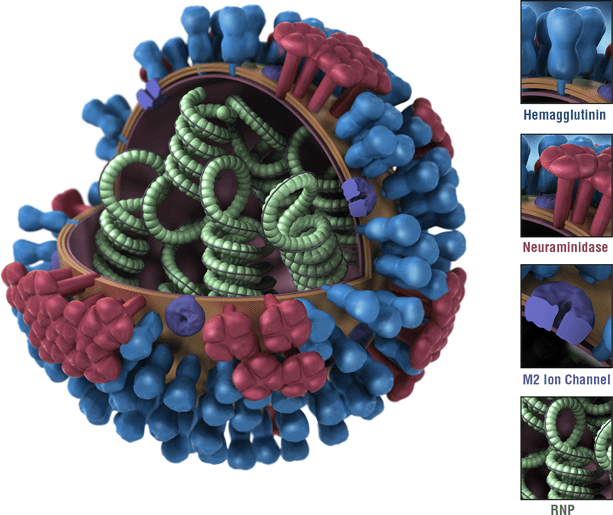
Dit is een afbeelding van een influenzavirus. De oppervlakte-eiwitten van het virus hemagglutinine (HA) zijn blauw afgebeeld. Het heeft van een influenzavirus zijn antigenen. De antigenen zijn eigenschappen van het griepvirus die door het immuunsysteem worden erkend en die een beschermende immune reactie teweegbrengen. De meeste griepvaccins zijn ontworpen om een immune reactie tegen het heeft van circulerende griepvaccins te veroorzaken.,
Er is een derde productietechnologie voor griepvaccins die in 2013 werd goedgekeurd voor gebruik op de Amerikaanse markt en waarbij gebruik wordt gemaakt van recombinant technologieexternal icon. Recombinante griepvaccins vereisen geen kandidaatvaccinvirus (CVV) om te produceren. In plaats daarvan worden recombinante vaccins synthetisch gemaakt. Om een recombinant vaccin te maken, verkrijgen griepactici eerst DNA, d.w.z. genetische instructies, voor het maken van een oppervlakte-eiwit genaamd hemagglutinine (HA) gevonden op influenzavirussen., HA is een antigeen, dat een kenmerk is van een griepvirus dat het menselijke immuunsysteem activeert om antilichamen aan te maken die specifiek op het virus gericht zijn. Dit DNA voor het maken van griepvirus HA antigeen wordt dan gecombineerd met een baculovirus, een virus dat ongewervelde dieren infecteert. Dit resulteert in een” recombinant ” virus. De rol van baculovirus is om de instructies van DNA voor het maken van griepvirus HA antigeen in een gastheercel te helpen vervoeren. Zodra het recombinante virus een gekwalificeerde lijn van de gastheercel van de Food and Drug Administration (FDA) ingaat, instrueert het de cellen om snel het antigeen HA te produceren., Dit antigeen wordt in bulk gekweekt, verzameld, gezuiverd en vervolgens verpakt als recombinant griepvaccin. Deze vaccins zijn dan kwaliteit en kracht getest door de FDA voorafgaand aan de FDA goedkeuring release van het vaccin partijen aan het publiek.
deze productiemethode vereist geen vaccinvirus dat in eieren wordt gekweekt en maakt in het productieproces helemaal geen gebruik van kippeneieren. Terwijl er andere vaccins op de markt van de V. S. zijn die gelijkaardige recombinante productieprocessen gebruiken, is er slechts één griepvaccin geproduceerd gebruikend recombinante technologie die door de FDA voor gebruik in de Verenigde Staten op dit ogenblik wordt goedgekeurd., Dit productieproces is het snelste omdat het niet wordt beperkt door de selectie van vaccinvirussen die zijn aangepast voor groei in eieren of de ontwikkeling van celgebaseerde vaccinvirussen.
CDC en FDA controleren de veiligheid van alle vaccins die in de Verenigde Staten zijn toegelaten, inclusief seizoensinfluenzavaccins. Meer informatie over de veiligheid van eigebaseerde, celgebaseerde en recombinante influenza, inclusief bijwerkingen, contra-indicaties en voorzorgsmaatregelen, screening en veilige toediening van het vaccin is beschikbaar bij seizoensinfluenza Vaccine Safety: A Summary for Clinicians.,
- De evolutie en revolutie van Griepvaccinenexterne icoon op de Amerikaanse Food and Drug Administration website.
- griepvaccin Researchexterne icoon op de website van het National Institute of Allergy and Infectious Diseases Institute, NIH.
- influenzavaccin voorschotten















