Grænser for Unge Sind (Dansk)
Abstrakt
Bakterier er meget lille, så lille, at du kan ikke engang se dem. Vidste du, at bakterier stadig kan blive syge, ligesom os? Faktisk inficerer de fleste vira i verden bakterier, ikke mennesker. Hvad sker der, når en bakterie bliver inficeret af en virus? Ligesom os har mange bakterier deres eget immunsystem, der hjælper med at forsvare sig mod infektioner. For nylig har forskere opdaget nogle nye bakterielle immunsystemer., Vi har været i stand til at genbruge disse systemer til helt nye anvendelser. Et sådant immunsystem, kaldet CRISPR, kan potentielt give os mulighed for at omskrive DNA, som vi ønsker, i enhver levende ting. Nu bruger forskere bakterielle immunsystemer som kraftfulde værktøjer til præcist at redigere DNA fra alle slags levende ting.
virus inficerer bakterier
vidste du, at bakterier kan blive syge, ligesom dig? Hvis du nogensinde har fået en forkølelse eller haft influen .a, ved du, at det ikke er sjovt at blive inficeret med en virus., Det viser sig, at de fleste vira i verden inficerer bakterier i stedet for mennesker. Forskere kalder disse vira bakteriofager (som bogstaveligt betyder “bakteriespisere”). Der er omkring 1030 vira i havet (det er en med 30 nuller bag det!). Det er flere vira end der er stjerner i universet! De fleste af disse havvirus inficerer bakterier .
måske er alt dette nyt for dig, men bakterier og vira har eksisteret i meget lang tid. Bakterier har udviklet sig sammen med vira siden livets oprindelse., De har været låst i en konstant kamp i over 3 milliarder år . Efter al den tid har bakterier udviklet sig et par tricks til at forsvare sig selv.
bakterier forsvarer sig, ligesom vi gør
din krop har mange måder at forhindre dig i at blive syg eller hjælpe dig med at blive bedre hurtigere, når du bliver syg. Din første forsvarslinje er din hud og membranerne inde i din krop. Disse holder ubehagelige bakterier og vira væk ligesom en mur. Når du får et snit, hvorfor skal du være forsigtig med at holde det rent? Så du ikke får en infektion.,
Nogle gange er din hud ikke nok, og du bliver syg. Når du får feber, er det et tegn på, at din krop forsøger at kæmpe, hvad der får dig til at være syg. Der er nogle kloge måder din krop kan bekæmpe infektion . Når din krop bekæmper en infektion med en virus for første gang, kan den danne en hukommelse om, hvordan den virus ser ud. På den måde ville du ikke blive syg af den virus igen. Du vil genkende den “dårlige fyr” og kæmpe tilbage. Vi kalder denne hukommelse “adaptiv immunitet”, og det er grunden til, at folk normalt kun får kyllingepokken en gang, og det er også grunden til, at vacciner fungerer., En vaccine viser din krop lidt af en død eller svækket virus, så din krop kan huske virussen og kæmpe mod den levende version senere. Nogle vira ændrer sig dog over tid, så disse minder ikke virker for evigt. Har du fået en forkølelse eller influen ?a mere end ?n gang? Det skyldes, at disse vira ændrer sig hurtigt. Hver gang du bliver syg, er det faktisk en lidt anden version af forkølelsen eller influen .aen.
bakterier virker meget enklere end os. De er trods alt meget små og består kun af en enkelt celle. Bakterier har ikke hjerner eller andre organer., Selv deres ene celle ser meget enklere ud end en af vores egne celler. Alligevel kan bakterier forsvare sig mod vira meget som vi gør.
først og fremmest er hver bakterie omgivet af en “cellemembran” og en “cellevæg.”Disse strukturer er som skjolde, der beskytter bakterier fra verden, ligesom din hud beskytter dig. Virus skal fastgøres til ydersiden af en celle og stikke igennem for at komme ind. Hvis bakterierne ændrer formen på deres cellevægge, kan dette forhindre, at vira klæber til dem. Derefter er bakterierne beskyttet mod infektion.,
Hvad sker der, hvis en virus kommer gennem en bakteries cellevæg? Nå, nogle bakterier har også adaptiv immunitet, ligesom vi gør! Det betyder, at de kan gemme en hukommelse om en virus for at hjælpe dem med at beskytte sig senere. Forskere opdagede kun dette relativt for nylig . Før troede ingen, at bakterier var komplekse nok til at have noget som adaptiv immunitet. Naturen fortsætter med at overraske forskere med nye, underlige ting. Vi kalder det system, der giver adaptiv immunitet i bakterier “CRISPR” – systemet.,
CRISPR står for “clustered regularly-interspaced short palindromic repeats”, hvilket er en kompliceret måde at beskrive, hvordan CRISPR ser ud. Da forskere sekventerede den genetiske kode for nogle bakterier (deres DNA), fandt de et mønster, hvor den samme korte sekvens blev gentaget igen og igen med nogle huller imellem (regelmæssigt interspaced). Disse korte gentagne bits var palindromer, hvilket betyder, at de så det samme fremad eller bagud (som ordene “kajak” og “racerbil”). Endelig blev alle gentagelserne fundet grupperet tæt på hinanden i det bakterielle DNA., Derfor kom forskerne op med navnet CRISPR. Vi indrømmer, at navnet er temmelig forvirrende, men jeg ville ikke bekymre dig om det, hvis jeg var dig. Forskere gør et OK job ved at finde ud af, hvordan verden fungerer, men vi er ikke gode til at komme med enkle navne på ting.
Hvordan virker CRISPR?
Hvad mener vi, når vi siger, at CRISPR hjælper bakterier med at “huske” en virus? Nå, for at forstå det, skal du først forstå, hvad en virus er. I modsætning til mennesker og i modsætning til bakterier er vira ikke lavet af celler., I stedet er en virus en flok DNA eller RNA (et molekyle relateret til DNA) pakket tæt ind i en kapsel lavet af proteiner. Du kan tænke på DNA som en lang bog, der beskriver, hvordan en levende ting skal være. For eksempel beskriver dit DNA, hvordan din krop skal fungere, og denne “kode” sammen med verden omkring dig former, hvordan du vokser. Alle levende ting gemmer deres genetiske kode som DNA, men nogle vira har RNA i stedet., RNA gør stort set det samme som DNA for virus, men er bygget lidt anderledes (tænk på koden for disse vira, der er skrevet på stentabletter i stedet for papir).
i begyndelsen af en infektion injiceres virusets DNA eller RNA i en celle (en human celle, hvis virussen inficerer mennesker, eller en bakteriel celle, hvis virussen inficerer bakterier). Bagefter omprogrammerer virussen cellen for at lave masser af kopier af virussen. Til sidst pakkes disse kopier i nye kapsler. Endelig er cellen brudt åben, og masser af nyfødte vira går ud i verden for at inficere nye celler., Du kan se, hvordan dette fungerer i Figur 1.
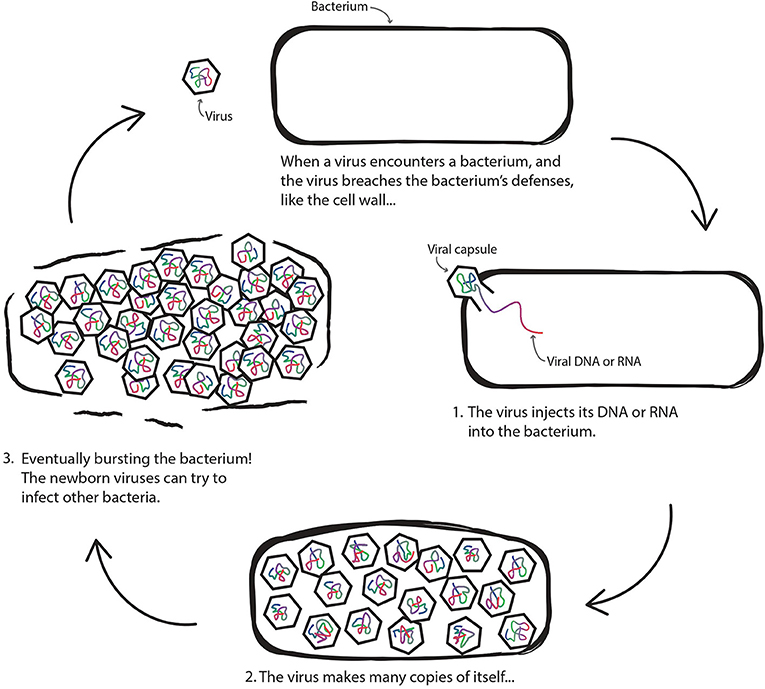
- Figur 1 – Hvordan en virus inficerer en bakterie.
CRISPR i bakterieceller arbejder i to trin. For det første, når en bakterie har et CRISPR-system, kan det gemme små stykker viralt DNA. Hver enkelt af disse stykker kan betragtes som en anden “hukommelse.”Nu kender bakterien en del af virusets “kode” og kan genkende den som en “dårlig fyr” senere., Hvis en virus sprøjter sig ind i en celle, og den virus matcher en af bakteriens lagrede minder, så ved bakterien, at der er noget galt. Når bakterien ved, at den bliver inficeret, starter den det andet trin med CRISPR-immunitet. Bakterien bruger sit CRISPR-system til at hugge virussen op, før virussen har en chance for at lave kopier af sig selv. Voila, ingen infektion! Vi viser, hvordan dette fungerer i figur 2. Selvfølgelig “tænker” bakterier ikke eller” kender ” ting som vi gør, fordi de ikke har hjerner., Alle trin i CRISPR-immunitet sker automatisk, men det er nyttigt at tænke på dem som “hukommelse”, når de prøver at forstå, hvordan de fungerer.
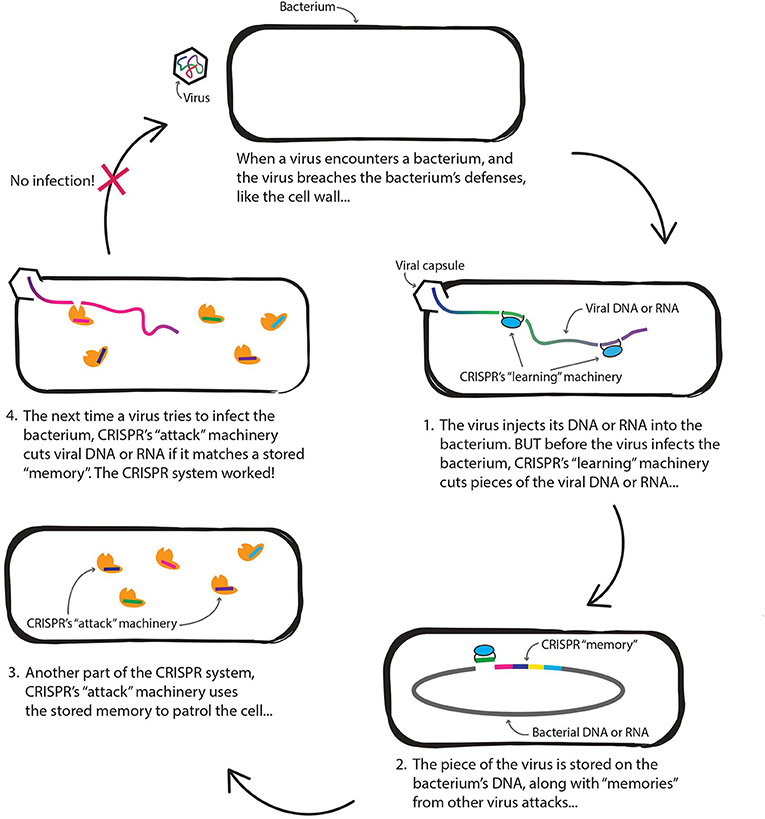
- Figur 2 – Hvordan CRISPR forsvarer en bakterie mod virus.
hvorfor bekymrer vi os så meget om CRISPR?
for nylig har CRISPR været i nyhederne meget. Folk er meget begejstrede for dette underlige lille system, som bakterier bruger til at bekæmpe vira! Hvorfor så meget spænding spørger du?, Det viser sig, at vi mennesker er ret gode til at stjæle de værktøjer, som bakterier har udviklet sig over milliarder af år og bruger dem til vores egne formål. Forskere har været i stand til at omdanne CRISPR til en måde at “DNA-redigering” på . Bakterier bruger CRISPR til at skære virusets DNA på en meget specifik måde. Forskere har fundet ud af, hvordan man bruger CRISPR til at skære noget DNA meget præcist på enhver måde, vi ønsker!
hvorfor vil forskere alligevel redigere DNA? Nogle menneskelige sygdomme er meget vanskelige at helbrede, fordi de er kodet ind i vores DNA. Disse sygdomme er ikke forårsaget af vira eller bakterier., Nogle eksempler er seglcelleanæmi og cystisk fibrose. Disse sygdomme er forårsaget af små ændringer i den genetiske kode. Disse ændringer får kroppen til at fungere lidt anderledes end den måde, den ellers ville. Med CRISPR kan vi redigere DNA og måske rette disse små ændringer. Dette betyder, at CRISPR kunne bruges til at hjælpe med at helbrede nogle af disse genetiske sygdomme. Det er dog ikke alt. Forskere bruger CRISPR til at designe hårdere afgrøder for os at spise, for at forsøge at slippe af med sygdomsbærende myg og meget mere.
Vi lærer stadig, hvordan man bedst bruger CRISPR som et værktøj., Det er vigtigt, at vi sørger for at bruge CRISPR af gode grunde. For nylig rapporterede en videnskabsmand, at han havde brugt CRISPR til at redigere DNA fra to børn. Han forsøgte at gøre dem resistente over for visse sygdomme. Det globale videnskabelige samfund var meget bekymret, da de lærte dette. Mange forskere var bekymrede over de anvendte videnskabelige procedurer. Andre tvivlede på, om forskeren havde handlet etisk. Mange forskere troede, at fordelen ikke opvejer risiciene. De sygdomme, som redigeringerne ville have forhindret, kan let forebygges med andre metoder., CRISPR-teknologi er ikke perfekt endnu og kan være skadelig. Ofte kan CRISPR indføre ændringer i DNA, hvor vi ikke ønsker det. Brug af teknologien på mennesker kan være risikabelt. Det er vigtigt at huske, at bare fordi en videnskabsmand kan gøre noget, betyder det ikke, at de burde. Forskere rundt om i verden holder ofte store møder for at diskutere disse spørgsmål og den bedste vej frem. På disse møder spørger de hinanden og offentligheden spørgsmål som: “er det nogensinde OK at redigere et menneskes DNA?”og” hvis ja, hvornår ville det være OK?”Hvad synes du?, Hvad hvis vi bruger CRISPR til at helbrede sygdomme? Hvad hvis vi bruger det til andre formål, som at gøre smartere eller stærkere mennesker? Hvad hvis kun nogle familier har råd til det? Det er vigtigt, at vi stiller hinanden disse spørgsmål, og at vi inkluderer berørte personer fra hele verden. På den måde kan vi vælge en sti, der bedre tager højde for alle involverede behov og bekymringer.
ordliste
Virus: en virus er en lille mængde DNA eller RNA omgivet af en proteinskal. Grundlæggende er en virus bare en brugsanvisning til opbygning af flere vira., Når virussen kommer ind i en levende celle (en menneskelig celle, hvis virussen inficerer mennesker, eller en bakteriecelle, hvis virussen inficerer bakterier) omprogrammerer den cellen og omdanner cellen til en virusfabrik.
adaptiv immunitet: alle organismer har forskellige typer immunitet for at beskytte sig mod infektion. Adaptive immunsystemer tillader organismer at huske infektioner fra fortiden for bedre at bekæmpe de samme infektioner i fremtiden.bakterie: en bakterie er en mikroskopisk organisme, der består af en enkelt celle. Deres celler er meget enklere end et menneskes, også., Nogle bakterier kan gøre dig syg, men de fleste gør det ikke. Faktisk stoler du på bakterierne i din tarm for at forblive sunde!CRISPR: CRISPR er et adaptivt immunsystem, som bakterier bruger til at bekæmpe virusinfektioner. CRISPR tillader bakterier at huske vira, de har set i fortiden, og genkende og bekæmpe disse vira i fremtiden.
DNA redigering: forskere har fundet ud af, hvordan man bruger CRISPR til at redigere DNA. Det betyder, at de potentielt kan omskrive “instruktionsmanualen”, der fortæller hver organisme, hvordan man kan leve og vokse. Vi kalder dette ” DNA-redigering.,”
Erklæring om interessekonflikt
forfatterne erklærer, at forskningen blev udført i mangel af kommercielle eller økonomiske forhold, der kunne fortolkes som en potentiel interessekonflikt.
Suttle, C. A. 2005. Virus i havet. Natur 437: 356. doi: 10.1038/nature04160
Chaplin, D. D. 2010. Oversigt over immunresponset. J. Allergi Clin. Immunol. 125: S3–23. doi: 10.1016/j.jaci.2009.12.980















