hur influensa (influensa) vacciner görs
- äggbaserade influensavacciner
- cellbaserade influensavacciner
- rekombinanta influensavacciner
För USA finns det tre olika influensavaccin produktionsteknik som godkänts av US Food and Drug Administration (FDA)extern ikon:
- ägg-baserat influensavaccin,
- cellbaserat influensavaccin och
- rekombinant influensavaccin.,
alla kommersiellt tillgängliga influensavacciner i USA tillverkas av tillverkare inom den privata sektorn. Olika tillverkare använder olika produktionstekniker, men alla influensavacciner uppfyller FDA: s säkerhets-och effektivitetskrav. Olika vacciner har olika indikationer. Se influensavacciner-USA, 2019-2020 influensasäsongen för specifika indikationer.
äggbaserade influensavacciner
det vanligaste sättet att tillverka influensavacciner är att använda en äggbaserad tillverkningsprocess
som har använts i mer än 70 år., Äggbaserad vaccintillverkning används för att göra både inaktiverat (avdödat) vaccin (vanligtvis kallat ”influensaskott”) och levande försvagat (försvagat) vaccin (vanligtvis kallat”nässpray influensavaccin”).
den äggbaserade produktionsprocessen börjar med CDC eller en annan laboratoriepartner i WHO: s globala övervaknings-och svarssystem för influensa som ger privata tillverkare med kandidatvaccinvirus (CVVs) som odlas i ägg per nuvarande FDA-regleringskrav., Dessa CVV injiceras sedan i befruktade hönsägg och inkuberas i flera dagar för att tillåta virusen att replikera. Det vätskeinnehållande viruset skördas från ägget. För inaktiverade influensavacciner (dvs influensaskott) inaktiveras vaccinvirusen sedan (dödas) och virusantigen renas. Tillverkningsprocessen fortsätter med kvalitetsprovning, fyllning och distribution. För nässpray influensavaccin (dvs levande försvagat influensavaccin-LAIV) är start CVVs levande, men försvagade virus som går igenom en annan produktionsprocess., FDA testar och godkänner alla influensavacciner före frisättning och leverans.
det finns flera olika tillverkare som använder denna produktionsteknik för att göra influensavacciner för användning i USA. Denna produktionsmetod kräver ett stort antal kycklingägg för att producera vaccin och kan ta längre tid än andra produktionsmetoder.
cellbaserade influensavacciner
det finns också en cellbaserad produktionsprocess för influensavacciner som godkändes av FDA 2012. Fram till nyligen började denna produktionsprocess också med äggodlade CVVs per FDA-föreskrifter., Den 31 augusti 2016 utfärdade FDA dock ett godkännande för Seqirus, den enda FDA-godkända cellbaserade influensavaccintillverkaren i USA, för att börja använda Cellvuxna CVVs. Cellbaserad tillverkning används för att göra inaktiverade influensavacciner (t.ex. influensa skott).
processen att skapa cellbaserade influensavacciner innebär flera steg. För det första använder CDC eller en av dess laboratoriepartners influensavirus som har odlats i celler för att göra CVVs, som sedan ges till en vaccintillverkare., Därefter vaccin tillverkaren inokulerar CVV i odlade däggdjursceller (i stället för i ägg) och tillåter CVV att replikera (dvs göra kopior) för ett par dagar. Därefter uppsamlas den virusinnehållande vätskan från cellerna och virusantigen renas. Tillverkningsprocessen fortsätter med rening och testning. Slutligen testar och godkänner FDA vaccinerna före frisättning och leverans.
cellbaserad influensavaccinproduktion kräver inte hönsägg eftersom vaccinvirusen som används för att framställa vaccin odlas i djurceller., Cellbaserad teknik har också potential för en snabbare start av influensavaccintillverkningsprocessen.
medan virus som använts under tidigare årstiders cellbaserade vaccin har odlats i celler, före säsongen 2019-2020 hade några av de virus som levererats till tillverkaren ursprungligen härletts i ägg. För influensasäsongen 2019-2020 är alla fyra influensavirus som används i det cellbaserade vaccinet cellderivat, vilket gör vaccinet äggfritt.
Mer information finns på CDC: s webbplats för cellbaserade influensavacciner.,
rekombinanta influensavacciner
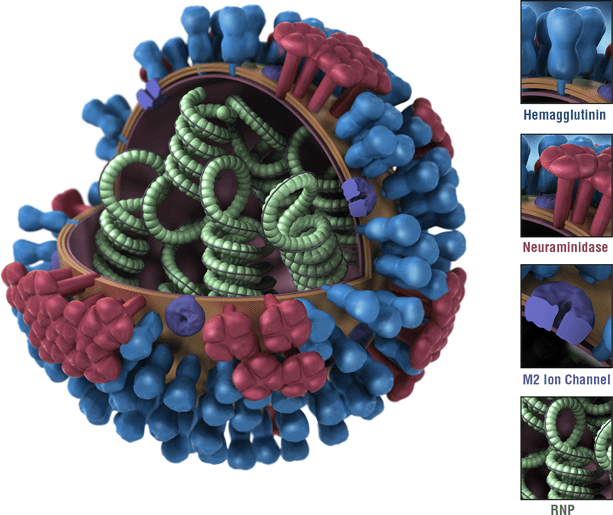
detta är en bild av ett influensavirus. Viruset ’ hemagglutinin (HA) ytproteiner avbildas i blått. Har av ett influensavirus är antigener. Antigener är egenskaper hos influensaviruset som känns igen av immunsystemet och som utlöser ett skyddande immunsvar. De flesta influensavacciner är utformade för att utlösa ett immunsvar mot HAs av cirkulerande influensavacciner.,
det finns en tredje produktionsteknik för influensavacciner som godkändes för användning på den amerikanska marknaden 2013 och som innebär att man använder rekombinant teknikextern ikon. Rekombinanta influensavacciner kräver inte att ett CVV-prov (candidate vaccine virus) produceras. Istället skapas rekombinanta vacciner syntetiskt. För att göra ett rekombinant vaccin erhåller influensaforskare först DNA, dvs genetiska instruktioner, för att göra ett ytprotein som kallas hemagglutinin (HA) som finns på influensavirus., HA är ett antigen, vilket är en egenskap hos ett influensavirus som utlöser det mänskliga immunsystemet för att skapa antikroppar som specifikt riktar sig mot viruset. Detta DNA för att göra influensavirus ha-antigen kombineras sedan med ett baculovirus, ett virus som infekterar ryggradslösa djur. Detta resulterar i ett ”rekombinant” virus. Baculovirusets roll är att hjälpa till att transportera DNA-instruktionerna för att göra influensavirus ha-antigen till en värdcell. När det rekombinanta viruset kommer in i en Food and Drug Administration (FDA) kvalificerad värdcelllinje, instruerar det cellerna att snabbt producera ha-antigenet., Detta antigen odlas i bulk, uppsamlas, renas och förpackas sedan som rekombinant influensavaccin. Dessa vacciner är sedan kvalitet och styrka testas av FDA innan FDA godkänner utsläpp av vaccin partier till allmänheten.
denna produktionsmetod kräver inte ett äggvuxet vaccinvirus och använder inte alls kycklingägg i produktionsprocessen. Medan det finns andra vacciner på den amerikanska marknaden som använder liknande rekombinanta tillverkningsprocesser, finns det bara ett influensavaccin producerat med rekombinant teknik som godkänts av FDA för användning i USA vid denna tidpunkt., Denna produktionsprocess är den snabbaste eftersom den inte begränsas av valet av vaccinvirus som är anpassade för tillväxt i ägg eller utveckling av cellbaserade vaccinvirus.
CDC och FDA övervakar säkerheten för alla vacciner som är licensierade i USA, inklusive säsongsinfluensavacciner. Mer information om säkerheten hos äggbaserad, cellbaserad och rekombinant influensa, inklusive biverkningar, kontraindikationer och försiktighetsåtgärder, screening och säker vaccinadministration finns tillgänglig på Säsongsinfluensavaccinsäkerhet: en sammanfattning för kliniker.,
- utvecklingen och revolutionen av Influensavaccinesexternal ikon på US Food and Drug Administration webbplats.
- influensavaccin Researchexternal ikon på National Institute of Allergy och Infektionssjukdomar Institutet, NIH webbplats.
- framsteg med influensavaccin















